Рекомендуется обратить внимание на элементы, находящиеся в пределах группы переходных металлов и некоторых неметаллов. Ключевыми кандидатами являются атомы, у которых на внешнем уровне электроны расположены в так называемых орбitalях, позволяя формировать неспаренные пары. Примеры таких веществ включают углерод, кислород и азот, в частности, их изотопы.
Для более точного анализа необходимо распознать электроны на уровнях s и p, а также учесть наличие пустых орбitalей. К примеру, углерод в своей электронной конфигурации имеет два неспаренных электрона, находящихся в p-орбитали, что открывает возможности для химических реакций. Также водород представляет интерес, так как его единственный электрон также не спарен.
С учетом вышеописанных аспектов, основное внимание следует уделять анализу конфигурации валентных электронов и возможности их спаривания. Таким образом, чтобы осуществить правильный выбор, необходимо учитывать также и электронные структуры соответствующих элементарных частиц.
Понятие неспаренных электронов в атоме
Элементы с высоким числом неспаренных частиц обладают определёнными химическими свойствами. В таких случаях важно учитывать, что уровень энергии открытых электронов влияет на реакционную способность и стабилизацию молекул и соединений.
Атомы с двумя несостоящими в паре электронами чаще всего относятся к группам элементов, которые находятся в p- и d-орбиталях. Примеры таких атомов: углерод и марганец. Углерод может иметь две неподелённые частицы, находясь на четвёртом уровне, в то время как марганец, находящийся на третьем уровне, также имеет два неспаренных электрона, что делает его реакционноспособным.
Наличие незаполненных орбиталей в атомной структуре способствует тому, что менее электроноотрицательные элементы легче образуют химические соединения. Это может быть полезным в синтетической химии и разработке новых материалов.
Важным аспектом является также то, что наличие неподелённых частиц может изменять магнитные свойства элементов, придавая им ферромагнитные характеристики. Это особенно заметно в переходных металлах.
При анализе таблицы Менделеева целесообразно обращать внимание на расположение элементов в группах и периодах, так как это влияет на количество неспаренных электронов и, соответственно, на их химическую активность.
Как определить электронные конфигурации элементов
Электронная конфигурация определяется расположением электронов в атоме. Для ее вычисления следует знать номер элемента в периодической таблице, так как он соответствует количеству протонов и, соответственно, электронов в нейтральном состоянии.
Работайте по системе Aufbau, чтобы расставить электроны по уровням энергии. Сначала заполняются самые низшие уровни. Используйте правила Паули и Хунда для правильного распределения электронов:
| Правило | Описание |
|---|---|
| Принцип минимальной энергии | Энергетические уровни заполняются с низших до высших. |
| Забор из двух электронов с противоположными спинами | На одном уровне на площадь не может находиться больше двух электронов. |
| Правило Хунда | При заполнении подуровней электроны сначала занимают отдельные орбитали, прежде чем будут спариваться. |
Для получения конфигурации выполните следующие шаги:
- Выясните порядковый номер. Например, для кислорода это 8.
- Используйте принцип Aufbau для распределения: 1s² 2s² 2p⁴.
- Проверьте количество электронов. У кислорода четыре электрона на второй энергии в подуровне p из шести доступных, что указывает на два неспаренных.
Убедитесь, что все конфигурации соответствуют указанным выше правилам. Это поможет вам легко находить информацию о любых других атомах, используя аналогичный подход.
Таблица Менделеева и электронаевские модели
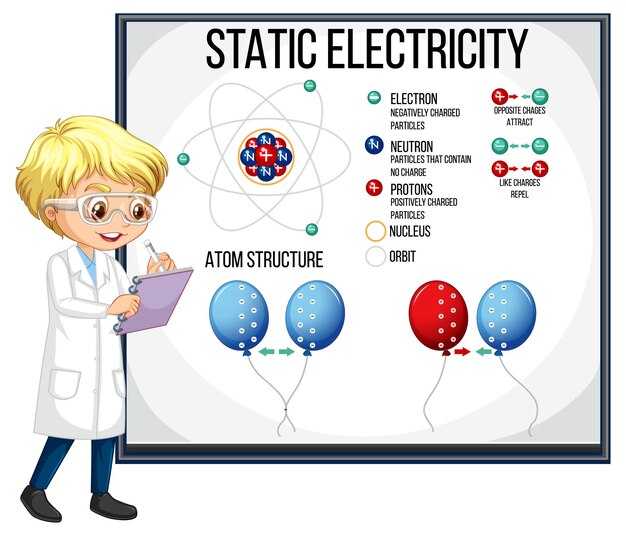
Для понимания характеристик химических веществ важно использовать периодическую таблицу. Например, углерод (C), кислород (O) и азот (N) следует выделить как элементы с двумя несопряженными электронами в своих валентных оболочках. Это связано с их электронной конфигурацией и размещением в таблице.
Сравнение нескольких электронных моделей, таких как модель Бора и квантово-механическая модель, позволяет четко видеть, как распределены электроны вокруг ядер. В последней модели особое внимание уделяется вероятностям нахождения электронов в различных орбиталях, что помогает предсказать химическое поведение элементов.
Среди ключевых моментов, на которые стоит обратить внимание: использование принципа Паули и правила Хунда. Важно, что соблюдение этих принципов дает возможность точно предсказывать свойства атомов и их реакции.
Электронные конфигурации других элементов также отмечают, например, фосфор (P) и сера (S), обладающие интересными свойствами из-за своей способности образовывать молекулы с двумя несопряженными электронами. Это открывает новые возможности для реакций и соединений.
Таким образом, периодическая таблица не только упрощает понимание свойств элементов, но и служит основой для применения электронных моделей, позволяя предсказывать поведение химических веществ в различных условиях.
Примеры элементов с неспаренными электронами

Азот (N) обладает тремя неспаренными электронами в своей внешней оболочке, что делает его особенно активным в химических реакциях.
Кислород (O) имеет два неспаренных электрона. Это определяет его реакционную способность при взаимодействии с другими веществами.
Фосфор (P) в своем основном состоянии демонстрирует три неспаренных электрона, что позволяет ему образовывать различные соединения.
Медь (Cu) имеет неспаренные электроны, которые обеспечивают ее проводимость и каталитические свойства. Особенно интересен ее один неспаренный электрон в 3d-орбитали.
Кобальт (Co) с тремя неспаренными электронами проявляет свои характеристики в образовании комплексов и магнитных свойствах.
Хлор (Cl) показывает один неспаренный электрон, который активно участвует в образовании химических связей.
Эти параметры влияют на химические свойства элементов и их реакционную способность. Изучение распределения электронов в последних оболочках критично для понимания химии и связанных процессов.
Методы визуализации электронных облаков

Для отображения распределения электронов вокруг ядра высокоэффективны три основных подхода: метод контурных линий, объемное отображение и моделирование квантовых состояний.
1. Метод контурных линий позволяет исследовать уровень вероятности нахождения электрона. На плоскости изображаются уровни, где присутствует одинаковая вероятность нахождения частиц. Это эффективно для гомоядерных систем.
2. Объемное отображение создает трехмерную репрезентацию облаков электронов. Используются графические системы, что позволяет визуализировать распределение в пространстве. Этот метод особенно полезен в изучении сложных молекул.
3. Моделирование квантовых состояний осуществляется через компьютерные расчеты, учитывающие волновую функцию. На выходе получаются детализированные изображения, которые демонстрируют, как электроны распределяются в зависимости от потенциальных полей.
Использование этих подходов помогает не только понять структуру молекул, но и прогнозировать свойства новых соединений. Их интеграция в научные исследования позволяет глубже изучать взаимодействия в химических реакциях.
Роль неспаренных электронов в химических реакциях
Неспаренные электроны играют ключевую роль в образованиях связей и реакциях, требующих взаимодействия между атомами. Например, элементы, обладающие одним или несколькими такими электронами, часто выступают в роли доноров или акцепторов в процессе обмена электронами. Это делает возможным образовывание ковалентных или ионных соединений.
При наличии одного неспаренного электрона возникает возможность для создания свободных радикалов, которые, хотя и нестабильны, способны инициировать цепные реакции и усиливать взаимодействия. Такие радикалы часто становятся инициаторами реакций в органической химии и в биологических процессах, таких как фотосинтез или клеточное дыхание.
Каждый конкретный элемент будет вести себя по-разному, в зависимости от его электронной конфигурации и положения в периодической таблице. Например, элементы группы 15, как азот, имеют три врожденных неспаренных электрона, что делает их активной частью различных процессов, включая синтез аминокислот.
Металлы, такие как железо, также могут быть классифицированы по наличию неспаренных электронов, что позволяет им участвовать в электрохимических реакциях. Например, в катализе железо может значительно ускорять реакции, увеличивая скорость образования конечных продуктов.
Таким образом, неспаренные электроны определяют реакционную способность соединений, их стабильность и возможности для взаимодействия с другими молекулами. Это открывает широкий спектр возможностей для синтеза новых материалов и соединений, влияя на развитие химической науки.
Элементы с полностью заполненными подуровнями
Элементы с полностью заполненными подуровнями характеризуются особой стабильностью и низкой реакционной способностью. В таблице Менделеева такие вещества находятся в конце каждого периода.
К ним можно отнести:
- Газообразные инертные компоненты: гелий, неон, аргон, криптон, ксенон и радон.
- Состояния благородных металлов: платина и золото, которые в своей электронной конфигурации достигают полной заполненности подуровней d.
- Элементы третьей группы: как, например, галий, содержащий полностью заполненные подуровни p, но также демонстрирующий своё химическое разнообразие.
Среди основных характеристик таких веществ выделяют:
- Низкую реакционную способность, что делает их идеальными для применения в различных технологиях.
- Высокую стабильность в различных условиях, что позволяет им сохранять свои свойства на протяжении долгих периодов.
- Часто используются в электронике и в производстве светодиодов благодаря своим уникальным свойствам.
Следует помнить, что заполненные подуровни не проявляют тенденций к образованию ковалентных или ионных связей, что значительно ограничивает их взаимодействие с другими атомами.
Как искать элементы с двумя неспаренными электронами

Начните с изучения конфигурации электронов. Необходимо определить, сколько электронов находятся на внешнем уровне. Это поможет выявить наличие неспаренных частиц.
Обратитесь к таблице Менделеева. Рассматривайте блоки s и p, так как именно в них вероятность наличия недостаточно связанных электронов выше.
- Элементы группы 1 (алкаличные металлы) содержат один неспаренный.
- Элементы группы 2 (щелочно-земельные металлы) на внешнем уровне имеют два электрона, которые могут быть спарены.
- Группа 13 (борная группа) с тремя электронами, где один из них остается без пары.
- Группа 14 (углеродная группа) и дальше – возможна комбинация с двумя неспаренными.
Используйте правило Хунда для оценки размещения электронов в подуровнях. Если на одном подуровне присутствуют электроны, они стремятся занять разные орбитали, пока не заполнится вся подуровень.
Обратите внимание на особенности переходных элементов. Здесь конфигурация 3d и 4s может привести к образованию неспаренных частиц.
Постепенно исключайте элементы с полной подуровней, так как они не обеспечивают неспаренности. Например, если подуровень заполнен (например, 3d10 или 4s2), то в нем не будет электрона без пары.
Также рассмотрите экзотические случаи с лантаноидами и актинидами, так как их поведение может отличаться от привычного.
Заключительным этапом будет проверка формул и теорий, таких как принцип Паули и правило Клечкова для подтверждения ваших наблюдений о непарных электронах.
Связь между периодической таблицей и количеством неспаренных электронов
Чтобы понять, сколько электронов без пары в атомах, необходимо учитывать их расположение в периодической таблице. Например, элементы, находящиеся в группах 1 и 2 (алкали и щелочноземельные металлы), имеют один или два электрона на внешнем уровне, что порой приводит к их неспаренности.
Переходными металлами являются особая категория, так как их электроны заполняют d-орбитали. Часто такие атомы содержат неспаренные электроны, например, в меди или железе можно встретить по одному отдельному электрону на d-орбитали.
С точки зрения электроотрицательности, неметаллы, расположенные вправо, например, кислород и азот, также демонстрируют неспаренные электроны в своих внешних оболочках. Это определяет их реакционную способность и образует характерные химические связи.
Размер атома напрямую влияет на количество несвязанных электронов, так как многие из них располагаются на более высоких уровнях энергии. Чем больше период, тем больше количество таких электронов, особенно в элементах, способных к образованию сложных соединений.
Следовательно, возможность существования несвязанного электрона зависит от группы и периода, в котором расположен элемент, а также от его электронной конфигурации. Используя эти данные, можно прогнозировать химические свойства веществ. Например, атомы с одним или тремя неспаренными электронами, как в случае с бором или алюминием, формируют определённые соединения с другими элементами.
Атомы переходных металлов и их электронические свойства
Переходные металлы характеризуются заполняемостью d-орбиталей, что влияет на их химические и физические свойства. В основном состоянии элемента с конфигурацией ns²(n-1)d⁴ наблюдаются два неспаренных электрона. Такие элементы, как хром (Cr) и ванадий (V), демонстрируют подобное поведение, что приводит к проявлению агрессивной химической активности и высоких значений магнитной восприимчивости.
Кобальт (Co) и марганец (Mn) также демонстрируют интересные признаки с тремя неспаренными электронами. Данная структура определяет их способность к образованию сложных соединений и катализаторных свойств. Открытые d-орбитали часто участвуют в образовании координационных соединений, что делает их универсальными в ряде применений в промышленности и исследованиях.
Таким образом, для определения наличия двух неподеленных электронов у переходных металлов следует обращать внимание на их электронную конфигурацию, где соответствующим числом будет n-1, равным количеству d-электронов в основном состоянии. Учет этих характеристик позволяет более точно предсказать реакционные способности и физические свойства различных соединений, образованных с участием переходных металлов.
Примеры, подтверждающие наличие двух неспаренных электронов
Примеры атомов с двумя электронами, которые не парные, учащаются в некоторых группах Периодической системы. Примеры включают:
- Азот (N): Элемент содержит 5 электронов. Распределение: 1s² 2s² 2p³. В 2p подуровне три электрона располагаются отдельно.
- Фосфор (P): Этот химический ингредиент также имеет 15 электронов. Конфигурация звучит как 1s² 2s² 2p⁶ 3s² 3p³, что приводит к трем неподелённым на 3p подуровне.
- Кремний (Si): Необработанный кремний обладает 14 электронами. Его электронная структура — 1s² 2s² 2p⁶ 3s² 3p², где два электрона на 3p подуровне расположены отдельно.
- Золото (Au): Этот элемент обладает 79 электронами, конфигурация [Xe] 4f¹⁴ 5d¹⁰ 6s² 6p¹ имеет один неспаренный электрон в 6p подуровне.
Следовательно, для определения наличия таких электронов полезно изучить электронные конфигурации. Определение неупакованных электронов в подуровнях s, p, d и f поможет отметить элементы с аналогичными характеристиками.
Дополнительные элементы с подобными свойствами:
- Кислород (O): 1s² 2s² 2p₄ — два электрона в 2p подуровне.
- Сера (S): 1s² 2s² 2p⁶ 3s² 3p⁴ — два электрона в 3p подуровне.
Использование этих конкретных примеров даст ясное представление о численности неспаренных электронов в различных атомах.
Как составить список элементов с двумя неспаренными электронами
Начните с определения валентных электронов для каждого из рассмотренных химических веществ. Обратитесь к периодической таблице, чтобы выделить группы и уровни энергий.
Сфокусируйтесь на элементах, находящихся в подгруппах d и p, так как именно они могут содержать неспаренные электроны. Обратите внимание на распределение электронов по orbitals.
Следующий шаг – это проанализировать электроны, находящиеся на внешнем уровне. Элементы с 2 или 3 валентными электронами чаще всего будут иметь два неспаренных, особенно среди переходных металлов.
Проверьте конфигурации электронов под внимание. Например, элементы, такие как железо (Fe) и ванадий (V), имеют два неспаренных. Они могут быть включены в ваш перечень.
Убедитесь, что вы изучаете только стабильные состояния, исключая возбужденные уровни, где распределение электронов может измениться. Убедитесь, что вы хорошо понимаете структуру периодической таблицы для точного анализа.
Итоговый список можно составить, собрав все подходящие вещества и записав их электронные конфигурации для окончательной проверки.